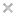|
|||
Примораживание кружки |
|||
|
Сегодняшний эксперимент взят из списка идей, которые предлагают наши посетители. Итак, для его проведения понадобится совсем немного реквизита: – плоская тарелка с налитой водой Берем тарелку с водой, ставим в нее кружку. Далее в кружку насыпаем снега и соли, и начинаем все активно перемешивать. Кружку при этом надо плотно прижимать к тарелке. Спустя примерно минуту кружка намертво примерзает к тарелке – можно спокойно поднимать их над столом. Говорят, еще более эффектно опыт выглядит, если приморозить кружку к табуретке – можно потом спокойно поднимать табуретку прямо за кружку. Ну и в заключение продолжим наш конкурс с домашними заданиями: Домашнее задание: исходя из видеозаписи, объясните данный эксперимент. Почему кружка примораживается? Какую роль выполняет соль? За наиболее развернутый ответ – бонус 50 рублей на телефон / электронный кошелек. |
Рассказать друзьям
| © | права на опубликованные материалы принадлежат их авторам |
Комментарии ( 3 )
-
Известно, что температура кристаллизации соленой воды чуть ниже температуры замерзания воды дистиллированной. Этот факт часто используется для борьбы с гололедом – улицы посыпают солью, в этом случае и снег, и лед начинают таять даже при отрицательной температуре.Артём 1 марта 2011, 02:00
Поэтому, если снег посолить, то он начинает активнее таять, а процесс плавления является очень теплоемким. Как следствие, соленый снег начинает активнее забирать тепло из окружающей среды – от кружки, которая в свою очередь, забирает тепло у воды в тарелке. Теплопроводностью окружающего воздуха в этом случае можно скорее всего пренебречь, поскольку она существенно ниже теплопроводности металла и воды.
Слой воды между кружкой и тарелкой достаточно тонкий, поэтому он достаточно быстро остывает до температуры, при которой находился снег в кружке – то есть до 0OC и превращается в лед, что и приводит к примерзанию кружки к тарелке. -
Будет еще лучше, если вместо соли взять, например, тиосульфат натрия (он же гипосульфит, Na2S2O3·5H2O), или глауберову соль, Na2SO4·10H2O), или их смесь. Используя тиосульфат, можно добиться охлаждения снежно–соляной смеси до –40 С.Кирилл Корабельников 2 марта 2011, 11:13 -
Ну что ж, более развернутых ответов тут сложно придумать. Бонус первому комментатору.Administrator 3 марта 2011, 18:03
Ваш комментарий